Japan (JA)
国・地域を選択してください。
SLMを用いた高機能多光子励起顕微鏡
2光子励起顕微鏡による生体深部観察
生物顕微鏡は、生物試料の表面の反射観察や、薄くスライスした生物試料の透過観察に用いられます。顕微鏡の対物レンズは、これらの観察で最も集光状態が良くなり、最高の光学性能が出せるように設計されています。また、細胞を観察する際には、細胞内部の小器官は同一色に近いかほぼ無色であるため、多くの場合は、観察したい対象のみを色素によって染色し、それが発する蛍光を観察する蛍光法が用いられます。
近年、医学・生物学の分野では、生物試料の深い部分を直接観察することが求められています。しかし、生物顕微鏡を用いて、厚い組織切片の深い位置を観察しようとすると、上記の設計条件から外れることと、観察対象そのもので光学的な歪みが発生することにより、対物レンズによる集光の品質が低下します。そのため、取得される蛍光画像にボケが生じ、分解能とコントラストが大きく低下します。
1990年に登場した、2光子励起蛍光顕微鏡は、生体深部を観察できる画期的なものです。この顕微鏡では、蛍光の発光に2光子励起という現象を用いています。通常の蛍光観察と比較し、2光子励起による蛍光観察では、蛍光の発光に用いる励起光に、生体透過性の高い近赤外の超短パルス光を用いるため、生体深部まで観察が可能です。また、励起光が対物レンズで小さく絞られた集光点付近でのみ発光するため、高い深さ分解能をもちます。これらの特長が生体深部の観察に有利に働いています。
登場から30年経た現在、撮像の高品質化に寄与するレーザ光源の高出力化や安定性の向上、より深い部位の観察を可能にする、生体を透明化する手法の開発など、さまざまな周辺技術が整い、2光子励起蛍光顕微鏡は生体機能の解明のために広く利用され始めています。
2光子励起蛍光顕微鏡の課題
2光子励起蛍光顕微鏡にも次のような課題があります。
(1)生体深部観察時に発生する収差によって画質が劣化する
(2)ポイント走査計測のため、計測時間が長い
(3)可視光レーザを用いる共焦点レーザ顕微鏡より解像度が低い
当社は空間光変調器(SLM)を用いて上記のような問題を解決し、高精度な深部観察を実現して、医学・生物学の研究に貢献することを目指しています。
SLMを用いた課題解決への取り組み
(1)生体深部観察時に発生する収差によって画質が劣化する問題
2光子励起蛍光顕微鏡では、超短パルス光を対物レンズで小さくして、時間的・空間的に光エネルギーを高密度に集中させることで、蛍光を発光させています。生体深部の観察では、対物レンズの設計条件から外れることと、生体の表面や内部で光が屈折を受けることにより、光学的な歪みが発生し、集光点がボケて光エネルギー密度が低下します。そのため、空間分解能が低下し、同時に蛍光の明るさも低下して、像の品質が大きく低下します。このような光学的な歪みを収差と呼びます。
生体深部でも高い解像度の画像を得るためには、この収差を補正して観察する必要があります。SLMを用いると、積極的に励起光の波面を制御して、生体深部で収差の影響なく集光させることができます。このとき大事なことは、どのような収差が生じているかを把握することです。収差は屈折率界面の屈折率差の影響を受けますが、屈折率界面の形状の影響も受けるからです。当社は、これまでに屈折率差により発生する収差の補正ならびに、試料の表面形状により発生する収差を補正する手法などを開発し、それが生体計測にも利用できていることを確認しています(図1)。
図1.透明化したマウスの脳(深さ1750 µm~1900 µm)を観察した時の血管像
生体試料の形状による収差を考慮して補正を行うと、従来の観察では見えなかった血管が鮮明になります(参考文献2)。
(a)当社で開発した収差補正方法を適用
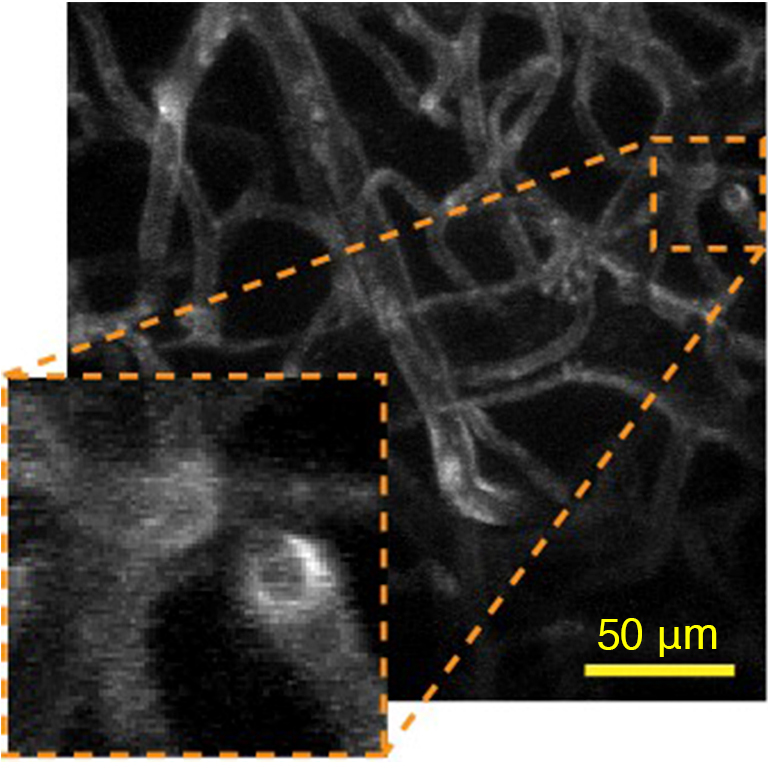
(b)収差補正なし

(2)計測時間が長い問題
生体の高速な現象を観察する場合、計測時間が短いほど有利になります。2光子励起蛍光顕微鏡はガルバノスキャナなどを用い、レーザ光を走査して画像を取得する方式が主流です。この走査撮像では、画照明の顕微鏡と比較して計測時間が長くなります。そこで、計測時間を短縮するため、励起光を多点に分岐して同時に撮像する、多点同時走査撮像方式を採用しました。この多点同時走査撮像は、SLMを用いて励起光の波面を制御することで集光点を複数作り、マルチアノード光電子増倍管のような複数箇所の同時検出が可能なデバイスと組み合わせて実現しました。励起光を4点に分岐することにより計測時間を1/4にできること、また撮像品質に影響がないこと、さらには収差補正と組み合わせて深部観察が可能であることを確認しています(図2)。
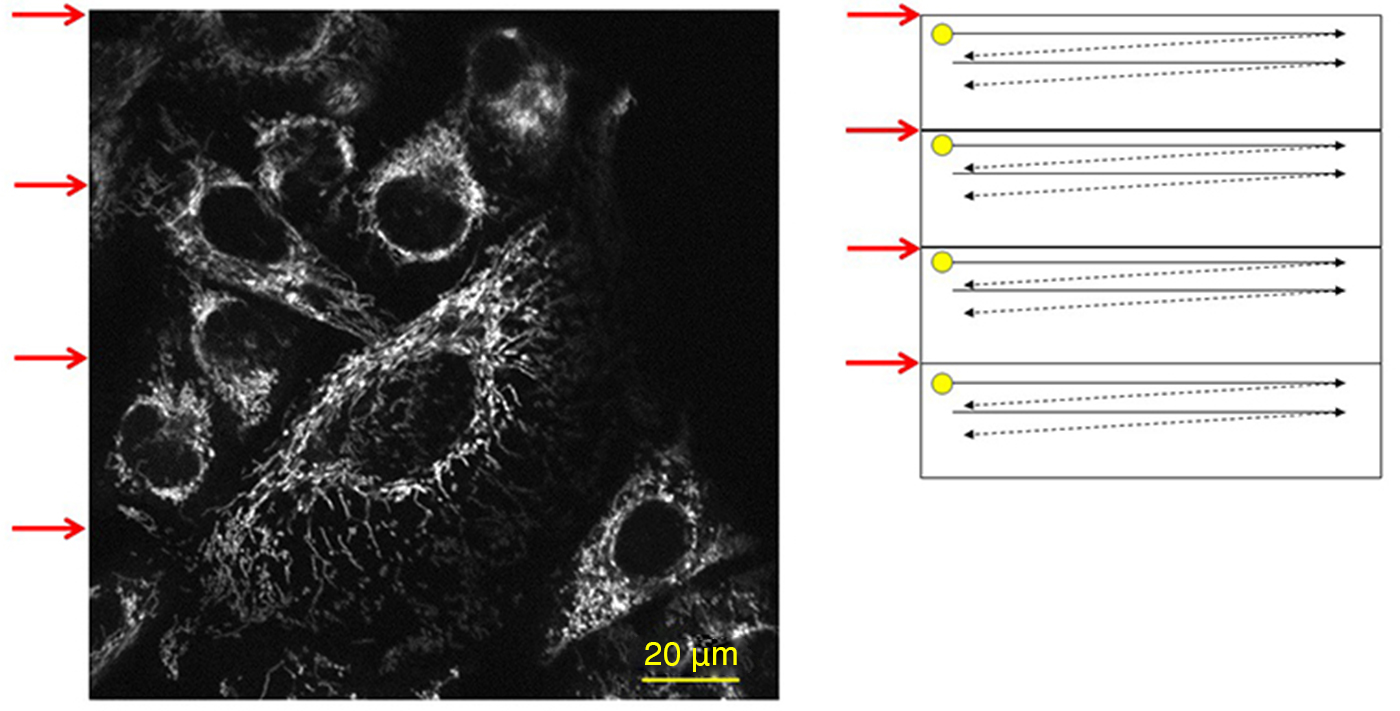
図2.ミトコンドリアをRhodamine 123で染色したHela細胞を観察して得られた蛍光画像
SLMで励起光を4分割して同時走査を行うことで、測定時間を1/4に短縮しました。
(3)可視光を用いる共焦点顕微鏡よりも解像度が低い問題
顕微鏡の解像度は、用いる光の波長が短いほど解像度が高くなります。2光子励起蛍光顕微鏡は励起光の波長が近赤外領域にあるため、生体透過性が高く、深い部位にまで達するという利点があります。しかし、励起波長が長いため、可視光励起である共焦点顕微鏡と比較すると解像度が低いという問題があります。当社は、2光子励起蛍光顕微鏡が有する深部観察の優位性を維持しながら、解像度を高める方法に取り組んでいます。これまでに、励起光の強度分布をSLMで制御することで解像度を向上させる手法を開発しました。
今後の目標
現在は、浜松医科大学と共同でこのSLMを用いた2光子励起蛍光顕微鏡の研究に取り組んでいます。これまでに、透明化方法に適した収差補正の開発や、腎臓を対象にした観察を実施してきました。
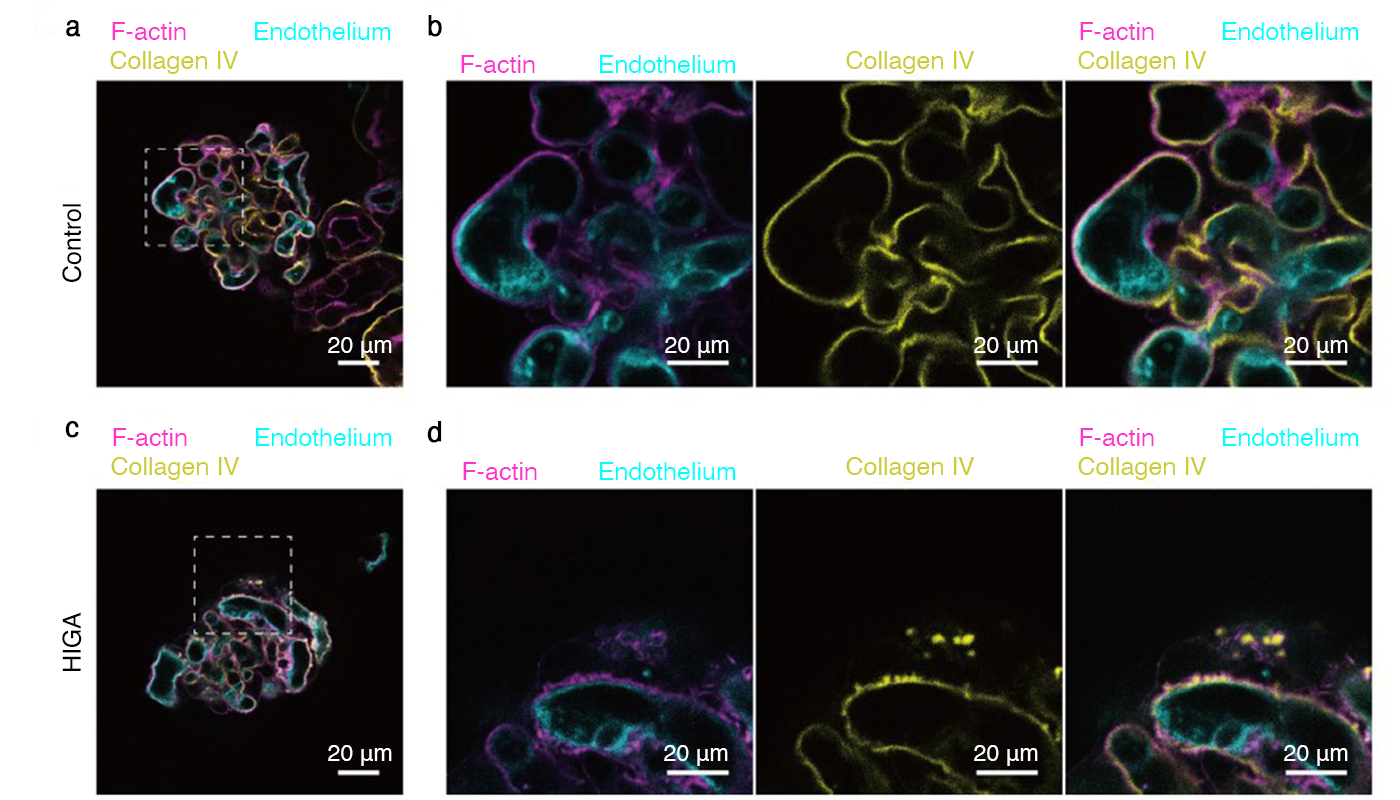
■野生型(control)と病態モデルマウス(HIGA)の腎臓を撮影した画像
腎臓計測では、従来の電子顕微鏡を用いた観察において確認されていた糸球内の血管上の突起物が、SLM搭載の2光子励起顕微鏡を用いることで、基底膜由来であることを明らかにしました(参考文献5)。
■3次元観察:透明化したマウスの腎糸球体観察
マウスの腎糸球体を摘出し染色した後、透明化処理を行い、3次元観察を行いました。糸球体を覆う細胞ポドサイト*を緑色、血管を赤色、核を青色に染色しています。動画では対物レンズを上下に動かしながら丸い糸球体の表面から深部まで観察しています。SLMで透明化溶液起因の収差を補正することにより、市販の水浸対物レンズを用いても深部まで観察することができます。
従来は糸球体をスライスして何枚ものプレパラートを作成し、光学顕微鏡で観察していましたが、スライスすることにより断面形状が劣化する、位置がずれるなどの問題がありました。2光子顕微鏡とSLMを用いることで立体的な組織を良好に観察することが可能となり、ポドサイト障害などの病態起因の形態変化をさらにとらえやすくなると考えています(資料提供:紺野 在様 浜松医科大学 微生物学・免疫学講座 助教)。
*ポドサイト:糸球体の周辺を覆い、ろ過機能の調整を行う細胞です。今回は1次突起が染色されています。
生体機能の解明のために、2光子励起蛍光顕微鏡は今後さらに広く利用されていくと考えられます。浜松ホトニクスのSLMは、顕微鏡を多機能化・高性能化することが可能です。当社はSLMならびにSLMを取り巻く周辺技術である波面制御やデバイス技術などを向上させ、今まで観察できなかった現象を発見できるようにすることで、医学・生物学の研究への貢献を目指していきます。
参考文献
- N. Matsumoto, T. Inoue, A. Matsumoto, and S. Okazaki, “Correction of depth-induced spherical aberration for deep observation using two-photon excitation fluorescence microscopy with spatial light modulator,” Biomed. Opt. Express 6(7) 2575-2587 (2015).
- N. Matsumoto, A. Konno, T. Inoue and S. Okazaki, “Aberration correction considering curved sample surface shape for non-contact two-photon excitation microscopy with spatial light modulator,” Sci. Rep. 9252 (2018).
- N. Matsumoto, A. Konno, Y. Ohbayashi, T. Inoue, A. Matsumoto, K. Uchimura, K. Kadomatsu, and S. Okazaki, “Correction of spherical aberration in multi-focal multiphoton microscopy with spatial light modulator,” 25(6), 7055-7068 (2017).
- N. Matsumoto, A. Konno, T. Inoue, K. Watanabe, and S. Okazaki, “Amplitude-modulation-type multi-ring mask for two-photon excitation scanning microscopy,” OSA continuum 4(6), 1696-1711 (2021).
- A. Konno, N. Matsumoto, Y. Tomono, and S. Okazaki, “Pathological application of carbocyanine dye-based multicolour imaging of vasculature and associated structures,” Sci. Rep. 10, 12613 (2020).
- Confirmation
-
It looks like you're in the . If this is not your location, please select the correct region or country below.
You're headed to Hamamatsu Photonics website for JP (Japanese). If you want to view an other country's site, the optimized information will be provided by selecting options below.
In order to use this website comfortably, we use cookies. For cookie details please see our cookie policy.
- Cookie Policy
-
This website or its third-party tools use cookies, which are necessary to its functioning and required to achieve the purposes illustrated in this cookie policy. By closing the cookie warning banner, scrolling the page, clicking a link or continuing to browse otherwise, you agree to the use of cookies.
Hamamatsu uses cookies in order to enhance your experience on our website and ensure that our website functions.
You can visit this page at any time to learn more about cookies, get the most up to date information on how we use cookies and manage your cookie settings. We will not use cookies for any purpose other than the ones stated, but please note that we reserve the right to update our cookies.
1. What are cookies?
For modern websites to work according to visitor’s expectations, they need to collect certain basic information about visitors. To do this, a site will create small text files which are placed on visitor’s devices (computer or mobile) - these files are known as cookies when you access a website. Cookies are used in order to make websites function and work efficiently. Cookies are uniquely assigned to each visitor and can only be read by a web server in the domain that issued the cookie to the visitor. Cookies cannot be used to run programs or deliver viruses to a visitor’s device.
Cookies do various jobs which make the visitor’s experience of the internet much smoother and more interactive. For instance, cookies are used to remember the visitor’s preferences on sites they visit often, to remember language preference and to help navigate between pages more efficiently. Much, though not all, of the data collected is anonymous, though some of it is designed to detect browsing patterns and approximate geographical location to improve the visitor experience.
Certain type of cookies may require the data subject’s consent before storing them on the computer.
2. What are the different types of cookies?
This website uses two types of cookies:
- First party cookies. For our website, the first party cookies are controlled and maintained by Hamamatsu. No other parties have access to these cookies.
- Third party cookies. These cookies are implemented by organizations outside Hamamatsu. We do not have access to the data in these cookies, but we use these cookies to improve the overall website experience.
3. How do we use cookies?
This website uses cookies for following purposes:
- Certain cookies are necessary for our website to function. These are strictly necessary cookies and are required to enable website access, support navigation or provide relevant content. These cookies direct you to the correct region or country, and support security and ecommerce. Strictly necessary cookies also enforce your privacy preferences. Without these strictly necessary cookies, much of our website will not function.
- Analytics cookies are used to track website usage. This data enables us to improve our website usability, performance and website administration. In our analytics cookies, we do not store any personal identifying information.
- Functionality cookies. These are used to recognize you when you return to our website. This enables us to personalize our content for you, greet you by name and remember your preferences (for example, your choice of language or region).
- These cookies record your visit to our website, the pages you have visited and the links you have followed. We will use this information to make our website and the advertising displayed on it more relevant to your interests. We may also share this information with third parties for this purpose.
Cookies help us help you. Through the use of cookies, we learn what is important to our visitors and we develop and enhance website content and functionality to support your experience. Much of our website can be accessed if cookies are disabled, however certain website functions may not work. And, we believe your current and future visits will be enhanced if cookies are enabled.
4. Which cookies do we use?
There are two ways to manage cookie preferences.
- You can set your cookie preferences on your device or in your browser.
- You can set your cookie preferences at the website level.
If you don’t want to receive cookies, you can modify your browser so that it notifies you when cookies are sent to it or you can refuse cookies altogether. You can also delete cookies that have already been set.
If you wish to restrict or block web browser cookies which are set on your device then you can do this through your browser settings; the Help function within your browser should tell you how. Alternatively, you may wish to visit www.aboutcookies.org, which contains comprehensive information on how to do this on a wide variety of desktop browsers.
5. What are Internet tags and how do we use them with cookies?
Occasionally, we may use internet tags (also known as action tags, single-pixel GIFs, clear GIFs, invisible GIFs and 1-by-1 GIFs) at this site and may deploy these tags/cookies through a third-party advertising partner or a web analytical service partner which may be located and store the respective information (including your IP-address) in a foreign country. These tags/cookies are placed on both online advertisements that bring users to this site and on different pages of this site. We use this technology to measure the visitors' responses to our sites and the effectiveness of our advertising campaigns (including how many times a page is opened and which information is consulted) as well as to evaluate your use of this website. The third-party partner or the web analytical service partner may be able to collect data about visitors to our and other sites because of these internet tags/cookies, may compose reports regarding the website’s activity for us and may provide further services which are related to the use of the website and the internet. They may provide such information to other parties if there is a legal requirement that they do so, or if they hire the other parties to process information on their behalf.
If you would like more information about web tags and cookies associated with on-line advertising or to opt-out of third-party collection of this information, please visit the Network Advertising Initiative website http://www.networkadvertising.org.
6. Analytics and Advertisement Cookies
We use third-party cookies (such as Google Analytics) to track visitors on our website, to get reports about how visitors use the website and to inform, optimize and serve ads based on someone's past visits to our website.
You may opt-out of Google Analytics cookies by the websites provided by Google:
https://tools.google.com/dlpage/gaoptout?hl=en
As provided in this Privacy Policy (Article 5), you can learn more about opt-out cookies by the website provided by Network Advertising Initiative:
http://www.networkadvertising.org
We inform you that in such case you will not be able to wholly use all functions of our website.
Close















































































































